
衛生福利部於2018年9月6日頒布「特定醫療技術檢查檢驗醫療儀器施行或使用管理辦法」(簡稱特管法)正式開放六項細胞治療技術。
自2026年1月1日起細胞治療技術納入「再生醫療法」子法「再生醫療技術及指定製劑管理辦法」,稱為「再生醫療技術」,如下表。
| 項目名稱 | 適應症 |
|---|---|
| 一、自體纖維母細胞治療 | 皮膚缺陷:皺紋、凹洞及疤痕之填補及修復 |
| 二、自體脂肪幹細胞治療 | 一、 慢性或滿六週未癒合之困難傷口 二、 占總體表面積百分之二十以上之大面積燒傷或皮膚創傷受損 三、 皮下及軟組織缺損 四、 退化性關節炎及膝關節軟骨缺損 |
| 三、自體 CD34+ selection 周邊血幹細胞治療 | 一、 慢性缺血性腦中風 二、 嚴重下肢缺血症 |
| 四、自體免疫細胞治療(包括 CIK、NK、DC、DC-CIK、TIL、gamma-delta T 之 adoptive T 細胞輸入療法) | 一、 血液惡性腫瘤,經標準治療無效 二、 第一期至第三期實體癌,經標準治療無效 三、 實體癌第四期 |
| 五、自體骨髓間質幹細胞治療 (bone marrow mesenchymal stem cell) | 一、 退化性關節炎及膝關節軟骨缺損 二、 脊髓損傷 |
| 六、自體軟骨細胞治療 | 膝關節軟骨缺損 |
尚寧生技致力於細胞治療技術研究,自2024年8月7日起經衛福部陸續審核通過以NK免疫細胞治療「實體癌第4期」及「第1至第3期實體癌,經標準治療無效」兩項適應症,提供病患高品質、高活性的NK細胞,以期盼能提升免疫功能、改善生活品質、減緩癌症惡化的進程並盼能延長病患的存活時間。
| 再生技術 | 癌別分期 | 合作醫院 | 大腸直腸癌 | 食道癌 | 胃癌 | 肺癌 | 肝癌 | 乳癌 | 攝護腺癌 | 腎細胞癌 | 惡性膠質瘤 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| NK細胞 | 1-3期 | 彰濱秀傳 |  |  |  |  | |||||
| 仁濟醫院 |  | ||||||||||
| 4期 | 童綜合 |  |  |  |  |  |  |  |  |  |
|
| 仁濟醫院 |  | ||||||||||
| 台北馬偕 |  |  |  |  |  |  |  |  |  |
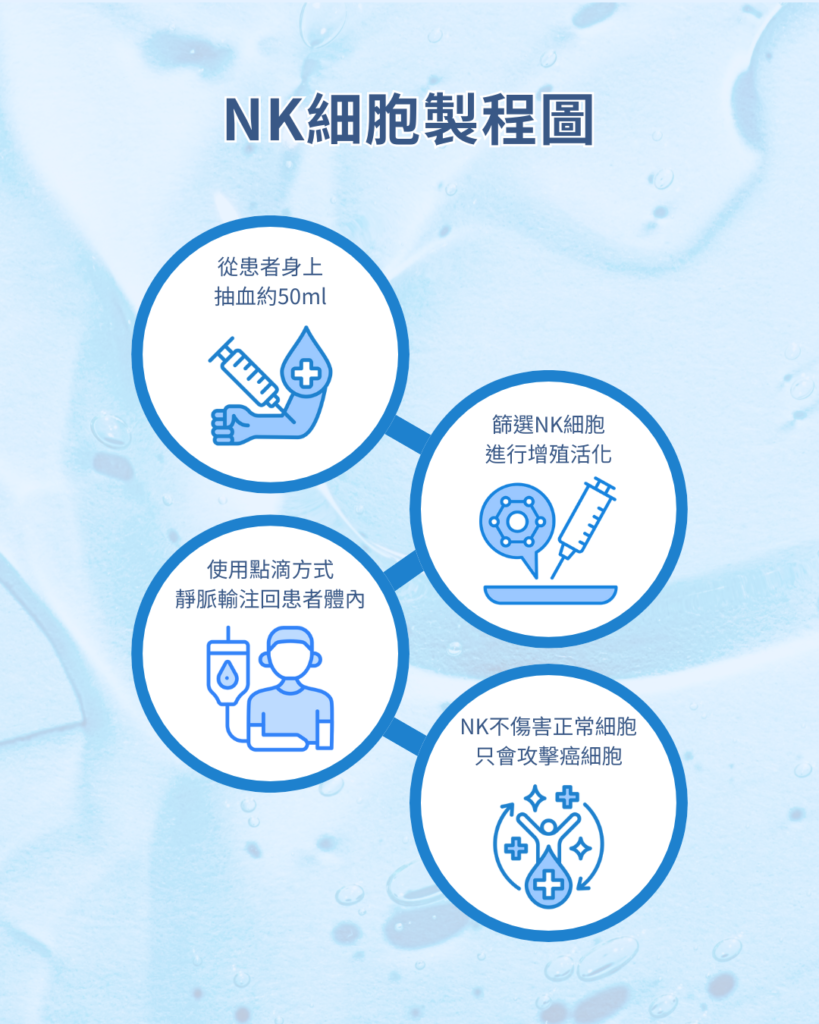
自體NK細胞治療為客製化治療,以病患本身的血液作為原料增殖NK細胞,每次抽血約50ml。此療程可併行現行治療,一個療程共六次NK細胞回輸。於完成最後一次治療後的第1、3、6、9及12個月,將由醫療團隊提供詳細的檢查與評估治療效果。
諮詢專線
童綜合醫院 04-2658-1919 #3922
彰濱秀傳醫院 04-781-388 #73633
台北仁濟醫院 02-23021133 #2510
尚寧生技臨床法規處 02-2793-8088 #635

